技術服務
TECHNICAL SERVICE
Fenton氧化技術
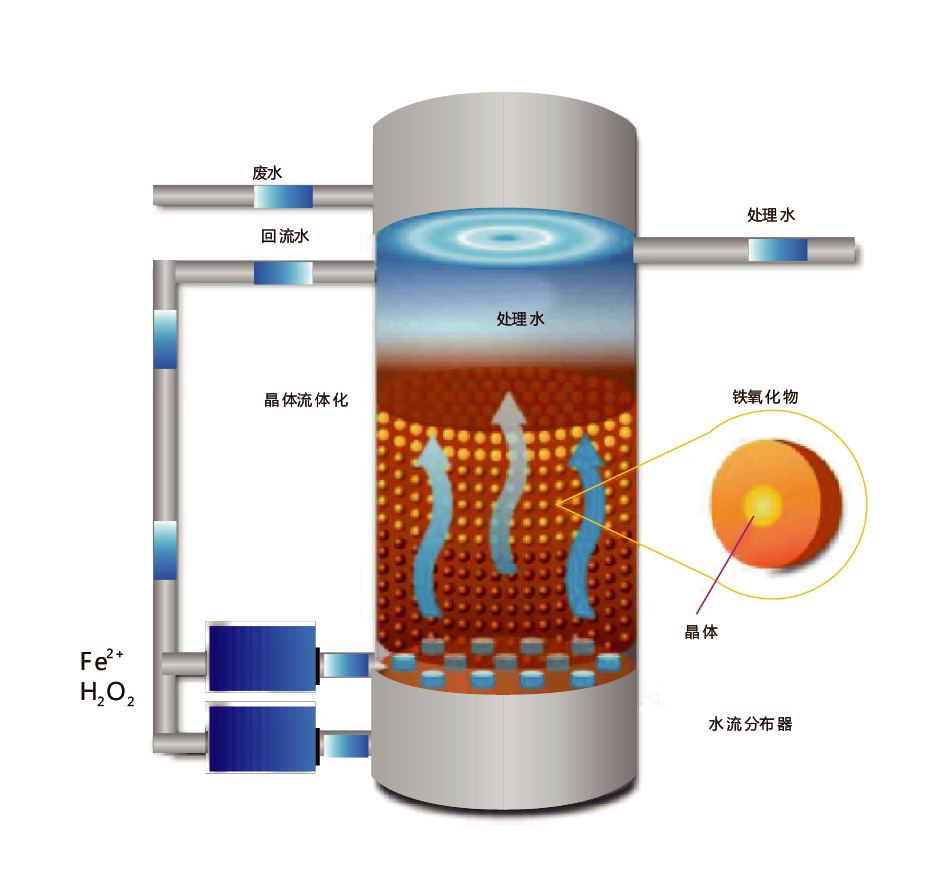
Fenton的氧化機理是在酸性條件下,過氧化氫在Fe2+催化劑作用下,產生兩種活潑的羥基自由基,從而引發和傳播自由基鏈反應,加快有機物和還原性物質的氧化。Fenton流化床處理技術是針對傳統Fenton法污泥產量太多的缺點加以改良,利用電場或結晶技術來提升處理效果及降低化學污泥產量,使適用范圍大為增加。
Fenton反應體系十分復雜,其關鍵是通過Fe2+在反應中起激活和傳遞作用,使鏈反應能持續進行,H2O2耗盡,其中產生的·OH自由基引發鏈式反應產生如HO2·等更多的自由基來降解有機物。Fenton試劑反應的主要過程如下:
Fe2++H2O2→Fe3++·OH+OH- (2-1)
Fe3++H2O2→Fe2++HO2·+H+ (2-2)
Fe2++·OH→Fe3++OH- (2-3)
Fe3++HO2·→Fe2++O2+H+ (2-4)
·OH+H2O2→HO2·+H2O (2-5)
Fe2++HO2·→Fe3++HO2- (2-6)
R·+·OH→ROH (2-7)
R·+H2O2→ROH+·OH (2-8)
R·+Fe3+→R++Fe2+ (2-9)
R++O2一ROO+……→CO2+H2O (2-10)
其中方程(2-1)是產生氧化劑·OH的主反應,為有利反應:方程(2-3)、(2-5)、(2-7)消耗了產生的·OH,方程(2-2)、(2-9)消耗了Fe3+,均為不利反應,必須加以抑制。Fe2+與H2O2之間反應很快,生成氧化能力很強的·OH游離基。與三價鐵共存時,由于Fe3+與H2O2反應緩慢地生成Fe2+,接著Fe2+再與H2O2迅速反應生成·OH,·OH與有機物RH反應生成有機R·游離基,R·進一步氧化,最終使有機物結構發生碳鏈裂變,氧化為CO2和H2O,從而使廢水COD值大大降低。
Fenton試劑除了產生·OH而具有強氧化性外,其還具有絮凝、沉淀功能,主要是因為在處理廢水過程中再生的二價鐵離子與氫氧化物反應生成了具有吸附、凝聚性能的鐵水絡合物。主要反應如下:
[Fe(H2O)6]3++H2O→[Fe(H2O)5OH]2++H3O+
[Fe(H2O)5OH]2++H2O→[Fe(H2O)4(OH)2]2++H3O+
當PH值為3~7時,上述絡合物變成:
[Fe(H2O)5OH]2+→[Fe(H2O)8(OH)2]4++2H2O
[Fe(H2O)8(OH)2]4++H2O→[Fe2(H2O)7(OH)3]3++H3O+
技術特點
具有極強的氧化能力,特別適用于生物難降解或一般化學氧化難以奏效的有機廢水的氧化處理。
除色、除味效果顯著,出水感觀明顯改善。
反應生成的鐵水絡合物可起到混凝作用,加強有機物去除效果。
中間流程設置循環系統,大大減少酸堿用量,降低運行成本。
填料表面形成的鐵氧體具有異相催化的效果,而流化床的方式亦促進了化學反應及傳質效率,使COD去除率提高。
運行成本低,是一般芬頓反應器的1/3左右。